近日,山东师范大学何洪彬/王洪梅教授在国际知名期刊Autophagy在线发表题为“EXOC5/SEC10 attenuates antiviral IFN-I signaling by targeting STING1 for autophagic degradation”的研究论文。

该研究建立在团队前期系列发现的基础上:包括SEC10通过负调控NRF2-ATF4-RIG-I信号轴抑制抗RNA病毒天然免疫反应(International Journal of Biological Sciences, 2025, 21(13):5744-5761.),SEC10通过促进STUB1介导的STAT1降解抑制I型干扰素(IFN-I)下游信号级联反应(PLOS Pathogens. 2025, 21(9):e1013472.)以及SEC10通过抑制KLF15介导的JAK1的转录激活促进病毒复制(Veterinary Microbiology. 2026, 316:111004.),进一步揭示了EXOC5/SEC10通过促进STING1蛋白的自噬降解,进而负调控I型干扰素(IFN-I)信号通路,促进DNA病毒复制的分子机制。
干扰素反应刺激因子(STING1)是DNA病毒识别通路CGAS-STING1中的关键适配蛋白,在抗病毒先天免疫中发挥核心作用。病毒感染后,STING1被激活并促进IFN-I和炎症因子的产生,进而清除病原体。STING1的蛋白稳定性及其信号强度的精细调控对维持免疫稳态至关重要。本研究发现,胞外分泌复合体亚基EXOC5显著抑制由HSV-1、HAdV-4及DNA类似物诱导的IFN-I信号通路。体外及体内实验表明,EXOC5促进病毒复制;在髓系细胞特异性敲除exoc5的小鼠模型中,IFN-I产生显著增强,小鼠对HSV-1感染的抵抗力和存活率明显提高。机制研究表明,EXOC5通过与E3泛素连接酶TRIM56相互作用,促进STING1在Lys224和Lys338位点发生K63连接的多聚泛素化修饰,该修饰作为自噬受体SQSTM1/p62的识别信号,介导STING1的选择性自噬降解,从而抑制IFN-I信号通路,促进DNA病毒复制。
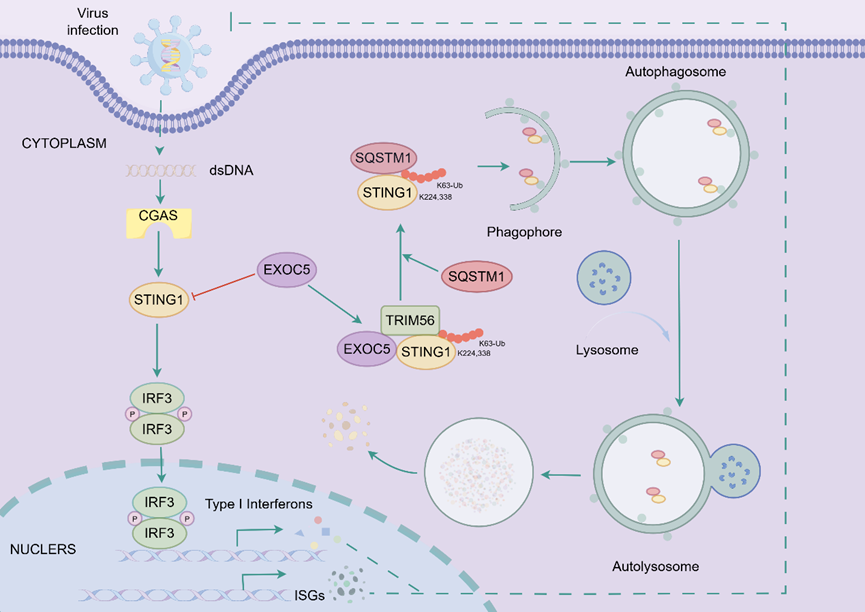
综上所述,该研究首次揭示了EXOC5-TRIM56-STING1-SQSTM1信号轴在抗病毒免疫中的关键作用,阐明了胞外分泌复合体亚基在先天免疫调控中的新功能,为开发靶向宿主免疫调控的抗病毒治疗策略提供了潜在新靶点。
山东师范大学为论文第一单位。何洪彬教授和王洪梅教授为文章的通讯作者。青年教师马文青和博士研究生徐亚男为文章的共同第一作者。该研究得到了国家自然科学基金、济南创新团队和山东省自然科学基金等资助。何洪彬教授与王洪梅教授团队长期从事动物病毒学及人兽共患传染病致病机制研究,专注于天然免疫、细胞自噬、细胞凋亡等,相关研究成果发表在Nature communication, PNAS, Autophagy,Cellular & Molecular Immunology,Advanced Science,Cell Death & Disease,PLOS Pathogens,Journal of Virology等国际知名学术期刊上。
供稿审核人:赵曰峰 马长乐
编辑:董广远
终审:巩 固

